La boisson gazeuse ou boisson carbonatée
Définition :
Une boisson est dite gazeuse ou carbonatée, si elle contient du gaz carbonique à l’état dissous. Ce gaz est appelé aussi : acide carbonique, CO2 ou anhydride carbonique.
La carbonatation est une opération qui consiste à dissoudre du gaz carbonique dans une boisson afin de lui donner son caractère de boisson gazeuse.
Cette dissolution peut s’opérer naturellement en produisant de l’acide carbonique au sein du liquide lors de sa fabrication par voie fermentaire et ce sera le cas de la bière, du cidre, du champagne. Elle peut aussi se réaliser en activant en milieu aqueux le mélange d’un acide organique et d’un carbonate, ce sera le cas des comprimés effervescents répandus en pharmacie qui contiennent en plus de la substance active de l’acide citrique et du carbonate de sodium à l’état anhydre.
Elle peut s’opérer artificiellement en introduisant du CO2 gazeux dans le liquide. Ce CO2 sera de provenance quelconque (Fermentation, combustion, chimique) et sera introduit au moyen d’appareillages appropriés (carbonateur).
C’est toujours avec du CO2 à l’état gazeux que va s’opérer la carbonatation proprement dite, et les formes liquide ou solide de ce corps, qui ne sont que des moyens commodes de stockage ou de transport sous un volume réduit, seront toujours ramenées à la forme gazeuse avant leur utilisation en carbonatation.

Molécule de CO2 musclée!
But de la carbonatation
La carbonatation confère aux boissons un certain nombre de qualités organoleptiques que le consommateur connaît bien et apprécie et qui sollicitent des organes sensoriels tels que :
Le goût : Le CO2 est un support de goût, il a une saveur acide, aigrelette et légèrement piquante qui sera perçue lorsque le gaz se dégagera dans la bouche. En même temps, en se dégageant, le gaz entraînera l’odeur et la saveur des essences et arômes volatils spécifiques incorporés dans le produit, et contribuera à augmenter la perception de l’odeur par les organes olfactifs du nez.
La vue : Citons pour mémoire les sens de la vue qui participe à la sensation générale en y apportant ce contentement éprouvé par les dégustateurs lorsqu’ils voient dans leur verre le gaz carbonique remonter en bulles à la surface de la boisson ou perler sur les parois internes du verre. Pour l’amateur de bière, rien n’est plus réjouissant que de voir la mousse fine et compacte, nourrie de bulles issues du fond du verre.
Enfin, le dégagement de CO2 a un léger effet anesthésiant sur les extrémités nerveuses de la parois buccale ce qui diminue et supprime même parfois la sensation de soif.
Taux de carbonatation des principales boissons carbonatées
Les bières traditionnelles anglaise sont réputées être les moins carbonatées avec 3 à 3,5 g de CO2 par litre. Cette faible carbonatation voulue pour un besoins spécifique gustatif de la boisson sera compensée aujourd'hui par l’azotage de la bière qui en introduisant de l’azote au sein du liquide avant son conditionnement permet grace à la finesse des bulles d’azote produites lors du remplissage du verre du consommateur d’obtenir une mousse importante et de qualité. A l’opposé, les bières belges sont souvent carbonatées à plus de 6 g/l et les bières de fermentations spontannées ou les bières de refermentation en bouteille peuvent atteindre des carbonatation de 7 à 8 g/l et plus, alors que la bière tirée à la pression a partir d’un fût dépasse rarement 4,5 g/l. Voir également notre article sur les techniques de carbonatation pour la bière.
Les eaux minérales gazeuses en contiennent de 4 à 6 g/l alors que les boissons gazeuses comme les Cola peuvent dépasser 9 g/l. Ce taux de carbonatation a été rendu nécessaire en ce qui concerne ces produits lors de la généralisation des récipients en plastique et notamment le polyéthylène téréphtalate (P E T). Car les récipients fabriqués avec ce matériau laissent apparaître dans le liquide une perte de gaz au cours du temps et notamment pendant le stockage de la boisson embouteillée. Pour pallier cet inconvénient les embouteilleurs augmentèrent le taux de CO2 de la boisson pour garantir en fin de D L V une carbonatation encore acceptable.
Le champion de la carbonatation reste le champagne avec 12 g/l de CO2 en moyenne.
Le Gaz Carbonique - Formule Chimique CO2
CO2 : Caractéristiques Physico-chimiques générales
Appelé dioxyde de carbone, anhydride carbonique ou acide carbonique.. Il est commercialisé et utilisé sous forme de gaz, liquide ou solide (neige carbonique). Pour l’industrie des boissons, il est vendu liquéfié à température ambiante sous sa propre pression de vapeur saturante (voisine de 70 bar) et logé en bouteilles en acier de 10 kg de gaz au maximum, ou vendu en réservoir réfrigéré basse pression à moins 20° C sous 20 bar de pression. Dans ce dernier cas le réservoir est a demeure chez le client et un camion citerne assure sa livraison, comme c'est le cas pour les gaz alimentaires pour brasseries d'Air Liquide. Les deux réservoirs (livraison et réception) sont équipés de moyens de régulation de la pression et de la température du gaz liquéfié.
Utilisé sous ses différentes formes, il aura en plus de son rôle dans la carbonatation des boissons, des applications protectrices sur la stabilité des aliments en chassant ou en se substituant à l’oxygène lors de leur conditionnement. Il aura également sous sa forme solide des utilisations dans le domaine frigorifique.
On peut déduire sa densité par rapport à l’air, de sa masse molaire M selon la formule :
d = M/29 ce qui donne Pour C = 12 et O = 16 - (12+ 16 x 2)/29 = 1,517
Son poids volumique à 0°C et à la pression atmosphérique normale est 1,98 (voisin de 2 g /l)
- Point critique : Température critique 31,1° C – pression critique 74,96 bars ; A cette température le CO² ne peut plus exister à l’état liquide quelle que soit la pression appliquée.
- Point triple : Température – 56,6° C – pression 5,28 bar ; A cette température et a cette pression les trois états : gaz, liquide et solide préexistent.
- Sa solubilité dans l’eau et les solutions hydro-alcooliques est importante.
A 15° C dans l’eau pure sous 1 bar de pression absolue, il se dissout à raison de 1 litre de gaz par litre de liquide ce qui correspond compte tenu de son poids spécifique à une dissolution de 2 g /l.
- A faible dose dans l’air respirable (< à 5%) il n’est pas toxique et réalise même l’activation des phénomènes respiratoires par excitation de centres cérébraux (deuxième souffle du coureur). Au-delà d’une concentration de 10% dans l’atmosphère il devient vite dangereux et est mortel à 20%.

Courbes donnant les limites de vaporisation, fusion et sublimation du CO2 en fonction de sa température et sa pression
LEGENDE
C= point critique T°=31°C – Sur BD liquide et gaz existent et la quantité de liquide augmente quand on se déplace de B vers D. Sur TT’ liquide, solide et gaz existent, T’ = point triple (P=5,28kg/cm2- T°= - 56,6 °C) A la pression atmosphérique (1 kg/ cm2) le liquide ne peut pas exister car la pression est inférieure à 5,28 kg/cm2.
LE CO2 à l’état de fluide super ou hyper critique
Le CO2 dans son état super critique c’est à dire T° >31° C et P > 78 bar à des propriétés de solvant importantes. Après extraction de la substance dissoute, il sera réutilisable par détente puis recompression.
Le CO2 sous forme de gaz hypercritique est utilisé dans l’industrie des boissons pour l’élaboration d’extraits de houblon, l’extraction d’arômes et la désodorisation de liège destiné à la fabrication des bouchons de bouteilles.
Remarque : Les fluides super critiques sont des gaz utilisés au delà de leur température et pression critiques. Ils présentent alors des propriétés solvantes très particulières qui peuvent être rendues spécifiques par simple variation de pression ou de température.
Les fluides supercritiques sont:
- Proches des liquides en masse volumique,
- Proches des gaz en viscosité,
- Entre gaz et liquides en propriété de diffusion.
Dans le cas du CO2 pris à l’état supercritique les avantages sont les suivants :
- Pouvoir solvant comparable aux solvants organiques.
- Haute diffusivité, basse viscosité, solvant apolaire.
- Pouvoir solvant ajustable par modification de pression et température.
- Absence de toxique dans les extraits et les résidus, milieu chimique inerte.
- Température et pression d’utilisation relativement basse (Tc 31,1 ° C - Pc. 72,8 bar)
- Aucun risque d’explosion.
- Faible coût d’exploitation.
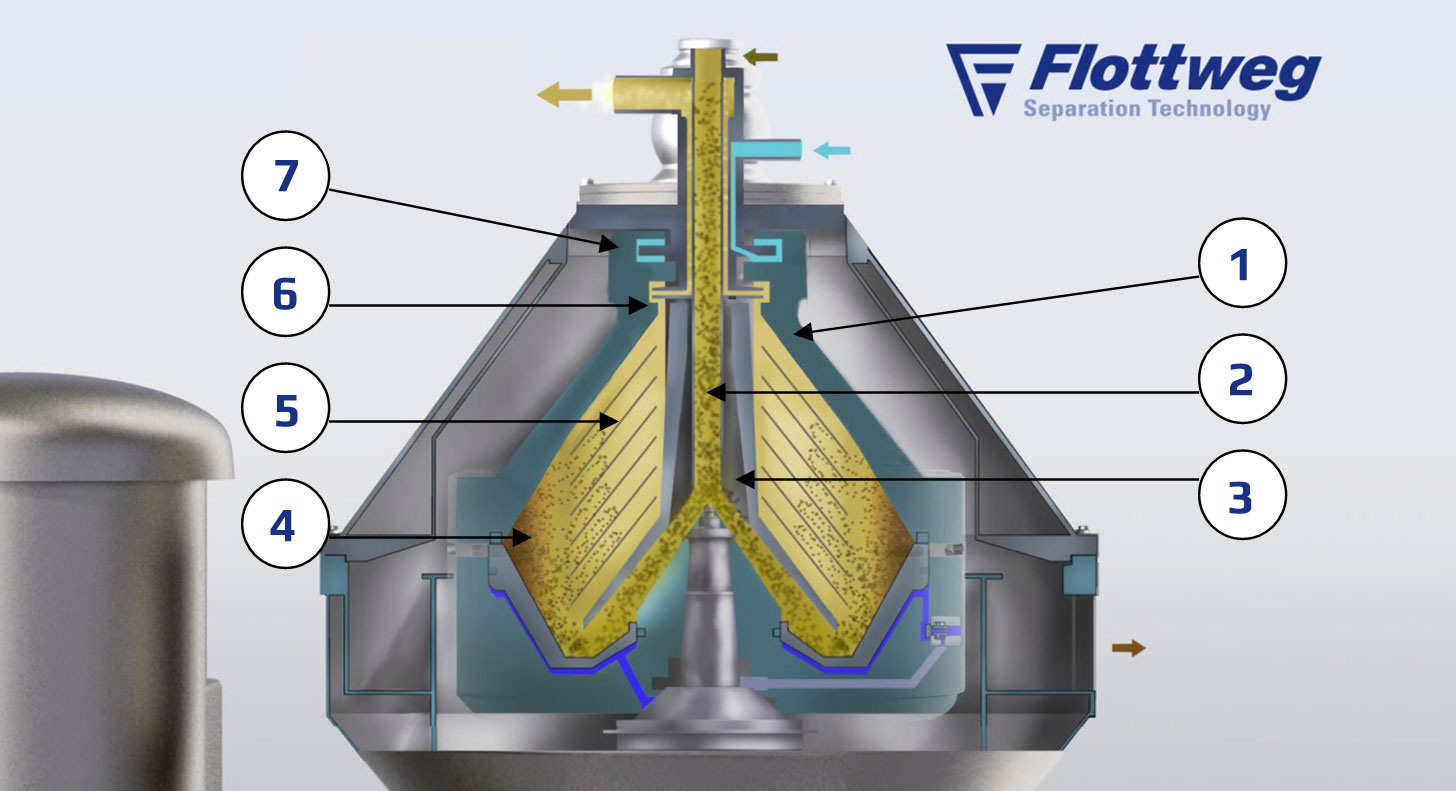
Le CO2 à l’état supercritique utilisé dans l’extraction des principes actifs du houblon est pour l’utilisateur brasseur le solvant idéal car il est très spécifique et ne dissout que les huiles essentielles, les acides alpha et bêta et les résines molles, laissant de côté les résines dures, les chlorophylles, et les poly phénols. L’extrait de houblon obtenu par extraction au CO2 supercritique a la couleur jaune de la lupuline et le parfum du houblon frais.Parfaitement à l’abri de l’air, l’extrait est protégé de toute oxydation.
Si la méthode supercritique classique avec des valeurs de P et T respectivement de 300 bars et 50 à 60 °C est très intéressante dans le cas de l’extraction du café, elle n’est pas indispensable pour le houblon, car l’augmentation de ces paramètres entraîne automatiquement une dissolution croissante des substances indésirables. Les paramètres suivants: 50 à 70 bars et une température voisine 31,5 °C conviennent parfaitement pour obtenir un rendement d’extraction supérieur à 95%. Le matériel utilisé avec cette méthode est évidemment le moins onéreux.

Diagramme d’extraction supercritique
Origines du CO2
Origine naturelle du CO2
Dans la nature on le rencontre dans l’air dans une proportion qui va croissant ; 280 ppm en 1850, 300 ppm en 1990.pour atteindre largement plus de 350 ppm aujourd’hui. Pourtant le taux de CO2 dans l’air devrait être maintenu constant par l’action combinée de :
- La photosynthèse par laquelle il est absorbé par les parties vertes des végétaux à chlorophylle sous l’action de la lumière et est transformé en amidon et en sucre. Pour cette fonction , la forêt amazonienne joue un rôle des plus important
- Du carbonate de Ca contenu dans les mers et où les récifs coralliens qui interviennent en jouant sur l’équilibre bicarbonates – carbonates pour réguler également la concentration en CO2 de la planète).
- Notre appareil respiratoire contient toujours du CO2 et nous le rejetons avec l’air expiré
- Il s’échappe du sol dans certaines sources naturelles, donnant naissance a des eaux minérales gazeuses qui seront renforcées ou non avec leur propre gaz.
Production industrielle du CO2
Production de CO2 par récupération de gaz de fermentation (exemple en brasserie)
- Hypothèse de base : Soit une bière à 12% plato et 80% d’atténuation réelle, ce qui correspond à 9,6 % plato de sucres fermentés. Par 100 cc de bière en fermentation on va disposer de 9,95 g fermentescible (Jeu du a et b des tables d’équivalence utilisées en brasserie. Les concentrations en g/100g plato sont transformées en g /100 cc)
D’après la réaction de la fermentation alcoolique :
C6H12O6 à 2CO2 + 2 CH3CH2OH +22kcal.
Le bilan massique montre que 1 g de sucre produit 0,488g de CO2
Les 9,95 kg de sucre fermentescible par hl vont donner : 9,95 x 0,488 = 4,855kg de CO2
Sur ces 4,855kg de CO2 une partie va être retenue pour la carbonatation de la bière à 5 g/l soit 0,5 Kg /hl. Il reste donc disponible 4,355kg/hl de CO2. En fait, compte tenu de des purges nécessaires pour chasser l’air qu’il contient, avant de mettre un tank de fermentation en récupération de CO2, du barbottage necéssaire au bondonnage , et les pertes diverses on va récupérer environ 3kg/hl.qui devront suivre un traitement de deshumidification ( gel de silice régénérable par air chaud), de désodorisation ( traitement au charbon actif ) et de liquéfaction à basse pression et basse température ( 20 bar et –20°C ) ou une liquéfaction haute pression
( 70 bar et 25 °C maximum), compte tenu de la température critique du CO2 située a environ 31°C.). Cette liquéfaction s’obtiendra par plusieurs étages de compression avec refroidissements succéssifs.

Récupération du CO2 par voie fermentaire (d'après FENART)
Production de CO2 par combustion de substances carbonées
Dans ce procédé, le plus utilisé industriellement, les gaz de combustion sont lavés, débarassés des cendres et du SO2 et absorbés sur un alcalin, puis désorbé par action thermique et envoyé dans un gazomètre en attente de liquéfaction
Production par calcination de carbonates ou leur traitement par un acide(récupération des gaz des fours à chaux ou à magnésie par exemple) décomposition du carbonate de chaux par la chaleur : CO3Ca → CO2+ CaO (chaux vive).
Comme déjà signalé, c’est également le cas de la production de comprimés éffervescents ou le produit actif est emprisonné dans un mélange anhydre de carbonate et d’acide citrique et réactivé en milieu aqueux.
Cette technique de production par action d’un acide sur un carbonate fut très usité autrefois pour obtenir ce gaz et l’utiliser pour la fabrication de boissons gazeuse. Le procédé est encore très utile dans les pays ou le CO2 liquéfié et commercialisé en l’état est inconnu.
Pratiques de l’utilisation du CO2 liquéfié

Principe schématique de l’approvisionnement de CO2 liquide par un camion citerne dans un réservoir basse pression maintenu à moins 20°C sous une pression de 20 bar. ( d'après Fenart )
Si c’est toujours sous forme gazeux que le CO2 sera utilisé dans l’industrie des boissons, comme déjà évoqué, il sera livré et approvisionné sous forme liquide soit en vrac à partir d’un camion citerne soit en bouteilles de 5 ou10 kg, ces dernières devront alors être stockées dans un endroit frais et couvert, en position couchée, ou debout “attachées”.
Dans le cas de la réception sous forme liquide réfrigéré (+20 bar, - 20°C). Le réchauffement éventueldu liquide stocké va provoquer une augmentation de la pression dans le réservoir. Cette augmentation sera combattue, en prèlevant du gaz dans la phase gazeuse du réserviur , ce qui provoquera la vaporisation d’une partie du liquide pour compenser le prélèvement de gaz et en conséquence refroidissement de l’ensemble. Le gaz prélevé sera recomprimé par un compresseur, refroidi et réinjecté dans le réservoir. D’autres système de régulation prévoient d’installer dans la phase liquide l’ évaporateur d’une machine frigorifique qui se mettra en route dès qu’un pressostat aura déterminé une augmentation de la pression dans le réservoir.
Avant de débuter le transfert du camion citerne de livraison au stockage chez le client utilisateur de gaz, il y aura lieu de mettre en comunication les deux phases gazeuses (réservoir à remplir, citerne de livraison) pour éviter la prise en neige carbonique du réservoir de livraison lors de la détente due à la vidange ..
Pour les bouteilles ou réservoir non calorifugés ni sécurisés de gaz carbonique liquide, la température de stockage devra être largement inférieure à la température critique de 31,1° C au delà de laquelle il y aura un risque d’explosion, le liquide se transformant spontanément en gaz et developpant alors une pression considérable. Bien sur, des sécurités existent sur ces récipients soit en autorisant une fuite de gaz par soupape soit tout simplement en réalisant spontanément une fuite au niveau du robinet de service provoquée par un manque d’étanchéité à la pression de sa liaison au récipient . Cette fuite est suivie d’une détente qui suffit à refroidir le liquide dans sa masse et baisser la pression dans le réservoir, pourtant des accidents ont déjà eu lieu avec des conséquences dramatiques.
Les bouteilles de gaz sont remplies en mettant en œuvre des pompes haute pression qui prélèvent sur la phase liquide d’un stockage, mais comme c’est toujours sous forme gazeux que le CO2 sera utilisé dans l’industrie des boissons. c’est sur la phase gazeuse de la bouteille que seront efféctués les prélèvements chez l’utilisateur. Si le prélêvement est rapide et continu, il va se produire là encore une détente du gaz et une vaporisation du liquide nécéssaire pour rétablir la pression de la phase gazeuse, ce qui risque de refroidir voire geler la robinetterie et empêcher de continuer le prélêvement, dans ce cas un arrosage de la bouteille à l’eau froide suffit généralement à stabiliser le débit de gaz. Surtout ne pas utiliser d’eau chaude à cause du risque de pouvoir atteindre la température critique.
Dans le cas d’un prélêvement par l’utilisateur a partir d’un réservoir basse pression ou haute pression d’un volume plus important, ( Stockage de 2T à 30 T de CO2 liquide ) le prélêvement se fera sur la phase liquide et nécéssitera d’avoir a vaporiser le liquide avant de l’envoyer vers l’utilisation, il faudra dans ce cas faire appel a des vaporisateurs qui sont des réchauffeurs fonctionnant à l’électricité ou à la vapeur et dimmensionnés pour un débit précis de prélèvement.
L’avantage de l’utilisation de CO2 liquéfié en bouteille, tient au fait que tant qu’il reste une goutte de liquide dans la bouteille, la pression à l’interieur de celle ci reste constante pour une température donnée, cela améliore les conditions de travail des détendeurs placés en sortie. Ce que l’on ne retrouve pas avec l’azote qui n’est pas liquéfiable aux températures d’utilisation et qui est livrée dans des bouteilles à plus haute pression, mais sous forme gazeuse et pour lesquelles la pression interne diminue au fur et a mesure du prélèvement.
MIX–GAZ
Les mix-gaz sont des mélanges de gaz alimentaires. Généralement il s’agit d’un mélange d’azote et de CO2
Utilisés dans le cadre du tirage pression de la bière, ils vont servir à appliquer sur le fût en tirage une pression totale qui sera composée d’une pression de gaz carbonique destinée à assurer le maintien de la carbonatation de la bière, et d’une pression d’azote destinée à vaincre les dénivellations depuis le fût jusqu’au robinet de tirage et les pertes de charge de la conduite de bière.
L’azote est utilisé car c’est un gaz neutre doté d’une très faible solubilité. De plus les bulles formées par l’azote au sein du liquide sont petites par rapport à celle produites par le CO2. Cela communique à la bière une mousse fine et crémeuse, très recherchée. A tel point que certains brasseurs pratiquent l’azotate de leur bière.
Si tout au début de la mise en route des mix - gaz on utilisait des bouteilles de mélange CO2 - N2 dans des proportions définies aujourd’hui on préfère faire le mélange directement à la cave ou se trouve le fut en tirage à partir de deux sources de gaz différentes.
On notera que le CO2 est toujours livré en bouteilles sous forme liquide alors que l’azote est livré sous forme gazeux à 200 kg de pression (il n’existe pas a l’état liquide aux températures d’utilisation).
Les mélanges utilisés sont : 60% CO2 40% N2 - ou - 40% CO2 et 60% N2
Cette utilisation permet d’appliquer des pressions de transfert importantes sans risque de sur saturation en CO2.
Notons que la production de N2 sur place par des techniques membranaires se développe dans les grandes installations de tirage pression.
Pierre Millet